銅と硫黄の化合実験
銅と硫黄の化合実験
実験日:2020年5月11日(月)
掲載場所:四中ホームページ,理科室前
※pdf版はこちら→銅と硫黄の化合実験 [3860KB pdfファイル]![]()
今回は銅と硫黄の混合物を加熱し,化合する実験を行いました。
化合の生徒実験としては2年生で鉄と硫黄を混ぜて熱するものがあります。
3年生のみなさんは覚えているでしょうか?かなり印象に残る実験です。
多くの人が腐卵臭を体感したことと思います。
今回の銅と硫黄の化合は,授業では演示実験(見せる実験)の場合が多いと思います(特に今回の方法の場合…)。
反応速度は「鉄+硫黄」よりも,今回の「銅と硫黄」の化合の方がずっと上です。
では,実験スタートです。
(1)まずは銅の粉末4.0gと硫黄の粉末2.0gを用意します。

(2)用意した銅と硫黄の粉末を,乳鉢と乳棒でよく混ぜ合わせます。

(3)試験管に混合物を入れ,スタンドに固定します。

・試験管の角度は45度。
・試験管の口の方向には立たない。
・部屋の換気に気をつける。
硫黄が空気中の酸素と反応すると有毒な二酸化硫黄が発生する。
・スタンドの周辺を段ボールなどで保護する(中身が吹き飛ぶかも)。
これで下準備が整いました。あとは加熱するだけです。
結果の前に,ここで今回の反応をまとめておきます。
銅と硫黄が反応して結びつくと新しい物質ができます。
何という名前の物質でしょう?
銅+硫黄で…,「銅硫黄」でしょうか。「硫黄銅」でしょうか。
物質どうしが結びついて新しい物質ができることを化合といいます。
そこで,「硫黄」と「銅」の間に化合の「化」を入れます。
ということで正解は…,
「硫化銅(りゅうかどう)」です。
「硫黄」の2文字目の「黄」を「化」に変えて「銅」をそのうしろにひっつけます。
※物質が硫黄と化合することを「硫化」といいます。
反応のまとめ(化学反応式)

銅原子:硫黄原子=1:1で化合します。
銅原子1個の質量は,硫黄原子1個の質量の約2倍なので,銅:硫黄=2:1の比率で反応させるとよいのです。

さて,では実験の続きです。
いよいよ銅と硫黄の混合物を加熱して,硫化銅をつくります。
(4)銅と硫黄の混合物を加熱する。

・混合物の上部を弱火で加熱する。
慎重にするならもう少し上の混合物がない場所を熱する。
・反応が始まったら火をどかす。
反応熱がまわりに伝わり,反応が自動的に続く。
・反応は一瞬。1秒前後で終了する。
速すぎて火をどかす時間がないかも。
(5)加熱開始(銅4.0g+硫黄2.0g)。

1で反応が始まり,その後すぐに音をたてて爆発した(2)。爆発後も反応は進む(3)。

反応が連鎖していき,1秒で終了。火はどかす余裕がなかった。
次は銅と硫黄の量を変えて行います。
銅を6.0g,硫黄を3.0gに増やします(銅:硫黄=2:1に変わりはありません)。
さらに,加熱部分を混合物の上部ではなく,混合物の真下にすることで,反応性が高まるようにします。
(6)銅6.0gと硫黄3.0gで実験。



1回目の反応と比べ,ずっと激しいことがわかる。 やはり反応速度は速く,1秒以内。
またもや途中で火をどかす余裕がなかった。
(7)反応後の物質 黒い物質が約1m先まで吹き飛んだ。

この黒色の物質が硫化銅(上の写真の右)。ボロボロで脆い(もろい)。
さて,今回の実験では銅も硫黄も粉末を使いました。
「銅の粉末」ではなく,「銅板」を使うと,もう少し穏やかに反応が進みます。
<銅板を使った実験方法>
1.試験管に硫黄の粉末を入れ,加熱する。
2.発生した硫黄の蒸気に,熱した銅板を入れて触れさせる。
今回のように粉末どうしで反応させると,銅と硫黄がふれ合う面積が大きくなるので,反応が効率よく進みます。
<イメージ図:左側が銅板,右側が粉末どうし>
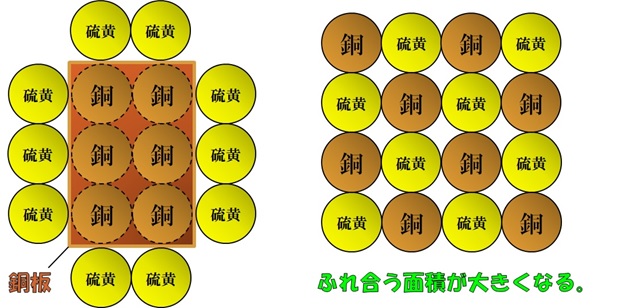
反応のまとめ

ところで,銅4.0gと硫黄2.0gを化合させたとき,できる硫化銅は何gだと思いますか?
ヒント:足し算だ!
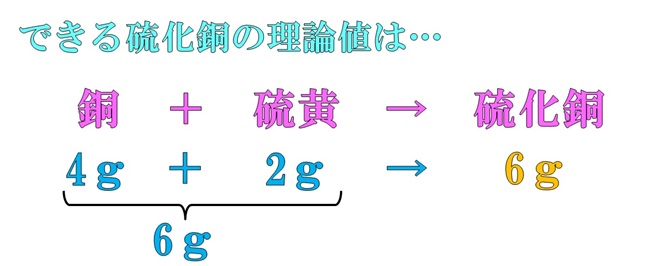
反応前の物質が[銅4.0g+硫黄2.0g]で合計6.0gですね。この合計量は反応後も同じです。
反応で何gかが消えたり,新しく増えたりはしません。
反応前後で物質の総量が変わらないことを質量保存の法則といいます。
ただし,実際には実験器具に粉末が付着する,硫黄の一部が酸素と化合して二酸化硫黄になるなどして,誤差が出ます。
なので,4.0g+2.0g=6.0gと正確にはなりません。
ちなみに,この反応は熱を放出する発熱反応です。
銅 + 硫黄 → 硫化銅(+熱)
なので,銅と硫黄の混合物の一部が反応すれば,そのとき生じた熱が未反応の混合物に伝わり,反応が連鎖します。
よって,途中で加熱をやめても反応は続きます。
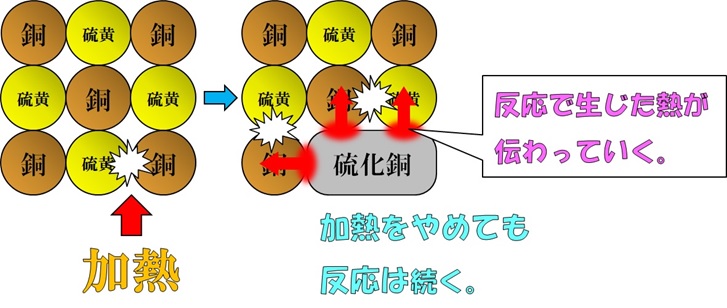
以上です。
編集:まつむら。
参考文献:『実践ビジュアル教科書 中学理科の化学』 福地孝宏 著 (誠文堂新光社)



